TANGELO: Studie bezpečnosti léku RO7248824

zdroje: forpatients.roche.com, clinicaltrials.gov
Studii TANGELO předcházela v USA pozorovací studie FREESIAS, kde se monitorovaly projevy a příznaky Angelmanova syndromu pro účely získání porovnávacích dat. Pacienti měli například dlouhodobě měřeno EEG, srdeční a dechovou frekvenci a jiné atributy během spánku pomocí speciální matrace v posteli v domácích podmínkách. Dále rodiče zaznamenávali záchvatové deníky apod.
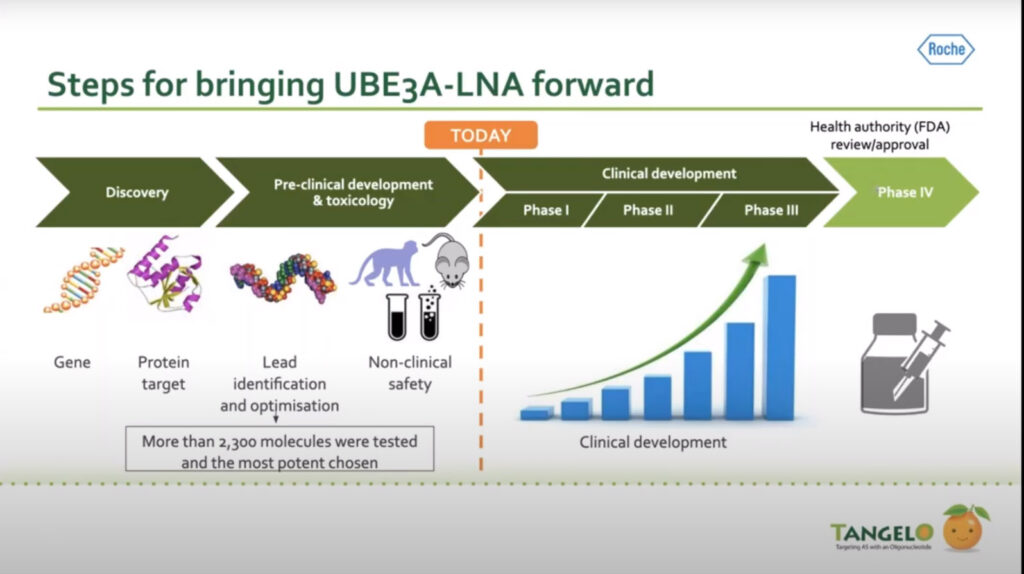
Souběžně probíhal dlouhý laboratorní výzkum a výběr vhodné látky. Z více než 2300 různých LNA molekul (Locked Nucleic Acid – molekula chemicky modifikovaná pomocí uzamčené nukleové kyseliny) byla vybrána jedna, která nyní postoupila k testování na lidech.
Molekula LNA v těle působí na gen UBE3A k produkování chybějícího proteinu UBE3A.
Výzkum na zdravých opicích prokázal zvýšení hladiny proteinu UBE3A.
Tvorba potřebného proteinu UBE3A v těle se děje na základě informace z matčiny části genu. Jedinci s Angelmanovým syndromem mají tento proces narušen (gen chybí nebo je zmutován) a proto protein nevzniká. Stejná informace jak protein tvořit je ovšem ukryta také v otcovské části genu. Při přepisu z genu je ale tato část informace standardně „zaslepena“ a nevyužije se. Molekula LNA je tzv. antisense oligonukleotid (podobně jako GTX-102). Váže se na malou část RNA, která je zodpovědná za umlčení otcovské části genu.

V červnu 2020 začala studie (fáze 1) na lidech TANGELO. Lék nese označení RO7248824. Aktuálně probíhá nábor pacientů.
Jedná se o otevřenou studii což znamená, že se nepoužívá placebo ani randomizace a všichni pacienti dostanou zkoumaný lék.
Cílem je získání dat o bezpečnosti, tolerabilitě, celkové působení látky v těle.
Cílem je zapojit 66 pacientů (ženy i muži) ve věkovém rozpětí 1-12 let.
Pacienti mohou mít genovou vadu způsobenou mutací nebo delecí (jiné varianty jsou vylučujícím kritériem). Studie probíhá v USA, Španělsku a Itálii ( celkem 17 center).
Časový průběh výzkumné léčby je následující:
- 6 týdnu screening (sledování pacienta),
- první dávka,
- po 4 týdnech druhá dávka,
- po 4 týdnech třetí dávka,
- sledování dalších 44 týdnů.
Studie v první fázi je plánována do konce roku 2022.
Lék se podává lumbální punkcí tedy injekce do míchy v oblasti beder, aby se dostal do mozku. Podává se v celkové anestezii (3x za 8 týdnů studie).
(nejedná se o odborný článek)

